Nature Machine Intelligence | 临港实验室合作构建AI驱动的肿瘤序贯治疗新策略,揭示表观药物增敏肿瘤治疗新机制
表观遗传异常是各类肿瘤的共性特征,但表观遗传抗肿瘤药物在应用中普遍面临疗效受限的困境,其症结在于:表观遗传调控本质上是伴随染色质重塑和转录重编程的动态演化过程,而当前的用药模式却大多停留在持续抑制靶点活性的静态逻辑中。从药理学视角审视,药物干预从来不是单行道——其在抑制靶点酶活的同时,必然触发细胞层面的代偿性响应,这些药物诱导的状态变化既是药效的延伸,更是治疗耐受的基础。因此,将该类药物治疗思路从持续压制转向动态调控转变,或可成为突破表观药物实体瘤疗效瓶颈的关键。
序贯治疗作为合理安排药物先后顺序,以顺应或调控肿瘤细胞演化的干预策略,正是实现这一思路的重要途径。然而,序贯治疗的优化设计面临诸多复杂挑战:药物应用顺序如何确定?不同药物间的时间窗口如何确定?临港实验室黄洵团队长期致力于表观遗传药物靶点发现与用药策略研究,建立了以逻辑与数据双驱动的表观药物科学研究体系。结合以上问题,团队建设的实时多模态药物反应检测集群(Real-time multimodal drug response detection cluster)涵盖了真实世界下中高规模的核酸,蛋白,细胞,类器官与体内模型,以自动或半自动化形式产生规模化的药物扰动数据集,为AI驱动的用药策略研究提供数据与验证体系。

黄洵团队与同济大学刘琦教授团队合作,聚焦抗肿瘤序贯治疗展开系统探索。近期在 Nature Machine Intelligence 期刊上发表论文,发布了结合肿瘤虚拟细胞和强化学习的序贯用药理性设计框架——SequenTx。该框架将序贯治疗设计为基于细胞状态演化的序贯决策问题,通过构建虚拟细胞(AIVC)模拟药物扰动下肿瘤细胞的变化,并结合强化学习进行策略优化,实现对药物序贯应用的系统性推演与方案筛选。在此基础上通过多维度实验揭示了表观药物处理诱导肿瘤细胞进入易感状态,进而增敏后续化疗的药物治疗新机制。
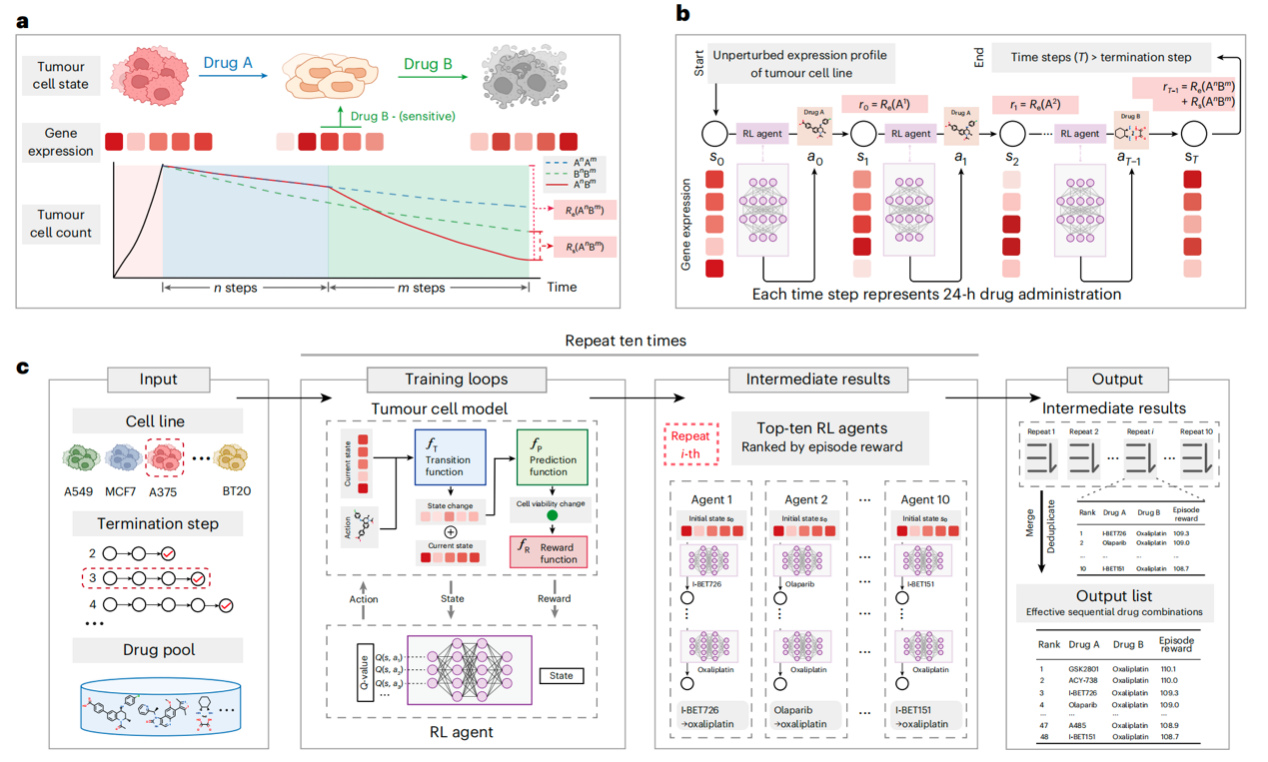
图1. SequenTx框架图
实验发现一:序贯组合中表观药物作为先导药物具有普适性诱导致敏效应
研究团队首先开展大规模体外泛癌种药物筛选,覆盖多种实体瘤细胞系及FDA获批抗癌药物库。对SequenTx推荐的序贯组合进行分析发现,在具有协同效应的方案中,作为先导药物出现频率最高的是以HDAC抑制剂为代表的表观遗传药物。这一规律提示,直接调控转录程序的药物优先应用,可为后续治疗创造有利条件。进一步验证表明,以BET抑制剂为代表的表观药物作为先导药物应用时,序贯组合可产生协同效应和稳定的基因表达变化。这表明表观药物可通过诱导转录重编程,将肿瘤细胞重塑为敏感状态,为后续化疗打开易感窗口。
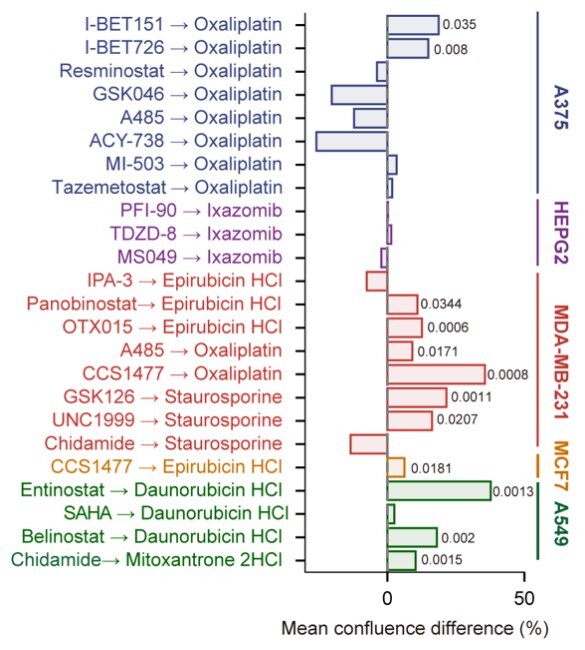
图2. 体外验证结果
实验发现二:给药顺序决定序贯疗效并揭示诱导致敏机制
基于体外筛选结果,研究团队在A375黑色素瘤小鼠模型中进一步比较了不同给药顺序的疗效差异。结果显示,BET抑制剂序贯奥沙利铂的治疗方案展现出显著的肿瘤生长抑制效果,验证了给药顺序在序贯治疗中的关键药理学意义。进一步机制研究发现,先导药物可诱导肿瘤细胞进入衰老状态,从而增强其对后续化疗的敏感性,形成诱导致敏的序贯协同模式。
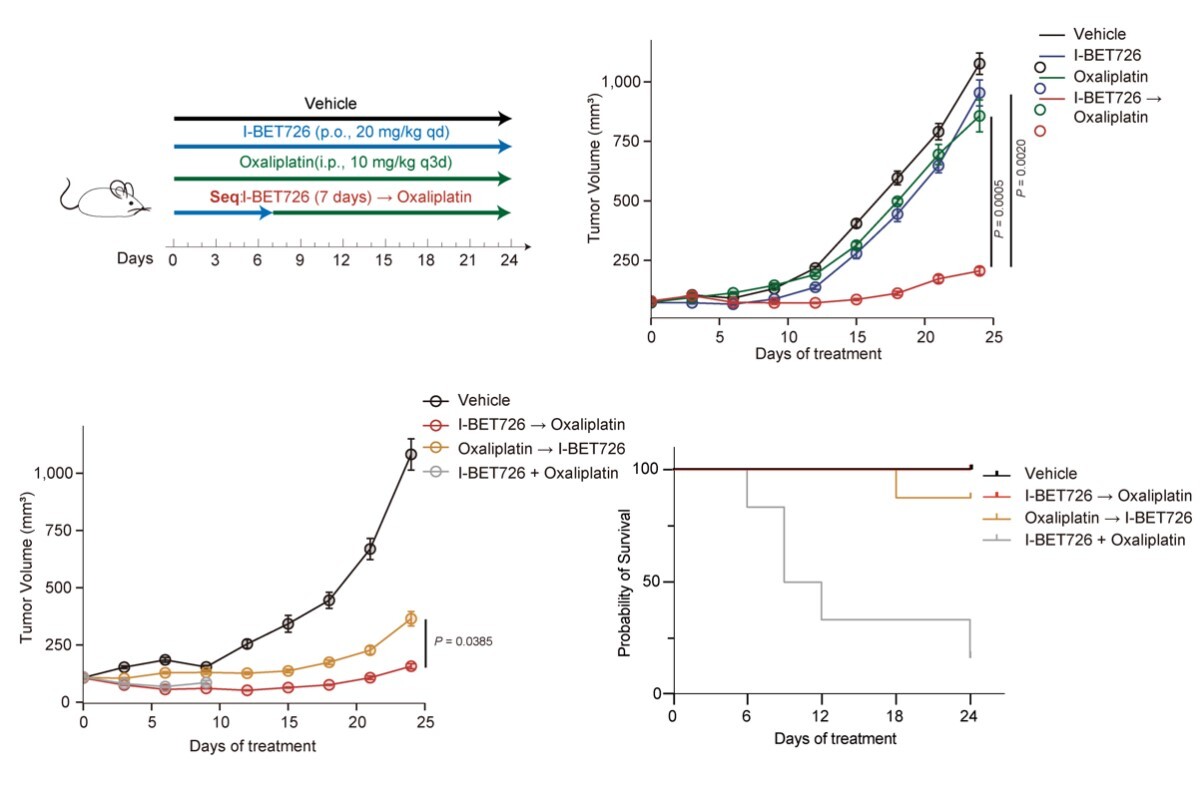
图3. 体内药效评价
综上所述,该研究针对序贯治疗优化设计的核心挑战引入AI方法进行理性推演,从表观药物实体瘤疗效受限的现实问题出发,并通过系统的平台进行药效和机制验证,成功发现了BET抑制剂+铂类化疗药这一具有协同效应的序贯方案。这一工作为表观药物在实体瘤中的应用开辟了新路径,提示表观药物的价值不仅在于单打独斗,也可作为先导诱导剂重塑细胞状态,为后续治疗创造机会窗口。同时,该研究也展示了从AI预测到推演实验验证反馈这一研究过程的可行性与有效性,为AI赋能肿瘤精准治疗策略的创新探索提供了有益借鉴。
临港实验室黄洵研究员、同济大学刘琦教授为本文通讯作者。同济大学博士陈晓涵、临港实验室与上海交通大学联合培养博士生邓玥为该论文的共同第一作者。本研究得到了临港实验室专项、国家自然科学基金项目、上海市东方英才计划领军项目等项目的资助。
附件下载:



