临港实验室合作构建三维病理学研究技术体系
传统病理诊断依赖二维切片“管中窥豹”,存在空间信息丢失、结构关联断裂的核心局限,亟需三维病理成像技术打开器官“黑箱”。随着生物医学研究对器官病变异质性认知需求的提升,临港实验室影像研究团队致力于构建三维病理学研究技术体系,综合运用多模态成像技术突破平面观测的局限性,为病理学研究提供跨尺度的空间解析维度。近日,该团队与中国科学院上海药物研究所合作在《Science Advances》《Advanced Science》等期刊连续发表系列研究成果,构建脑、肝、肺高精度三维病理图谱,为疾病机理、肿瘤治疗、靶向药物递送及药物评价等研究提供革命性工具。三维病理成像技术结合多尺度融合的影像分析,进一步推动了病理学研究从“平面观测”向“立体解析”的范式升级,构建起多尺度、多参数融合的新型病理学研究体系。这种能力的突破不仅拓展了传统病理学的研究维度,更通过建立器官病变的三维空间坐标框架,为系统解析疾病演进机制提供了关键支撑。
● 厘米级器官全景成像:实现小鼠脑、肝、肺等完整器官的三维重构
● 微米级细胞定位:精准捕捉细胞层面病理结构变化与药物递送轨迹
● AI量化分析系统:自动识别病理特征并建立空间定量评价体系
该技术首次揭示“疾病的空间密码”——胶质瘤血管侵袭的立体动态、肝纤维化以中央静脉为轴心的梯度病变、肺靶向药物在气管外壁的聚集规律,从根本上改变了“以二维切片推演三维疾病”的传统认知范式。
1. 构建脑胶质瘤高精度图谱,解析肿瘤异质性与纳米粒瘤内3D分布特征

本研究中临港实验室殷宪振团队与中国科学院上海药物研究所张继稳、张小川团队合作,构建不同阶段脑胶质瘤的亚微米级高精度3D图谱,实现全脑尺度肿瘤血管系统与细胞构筑的3D可视化,重点解析肿瘤血管病理重塑特征、血脑屏障通透性动态变化及纳米粒子 - 肿瘤微环境交互关系,从而为阐释肿瘤微环境与药物递送系统的互作关系提供清晰、直观的认识。
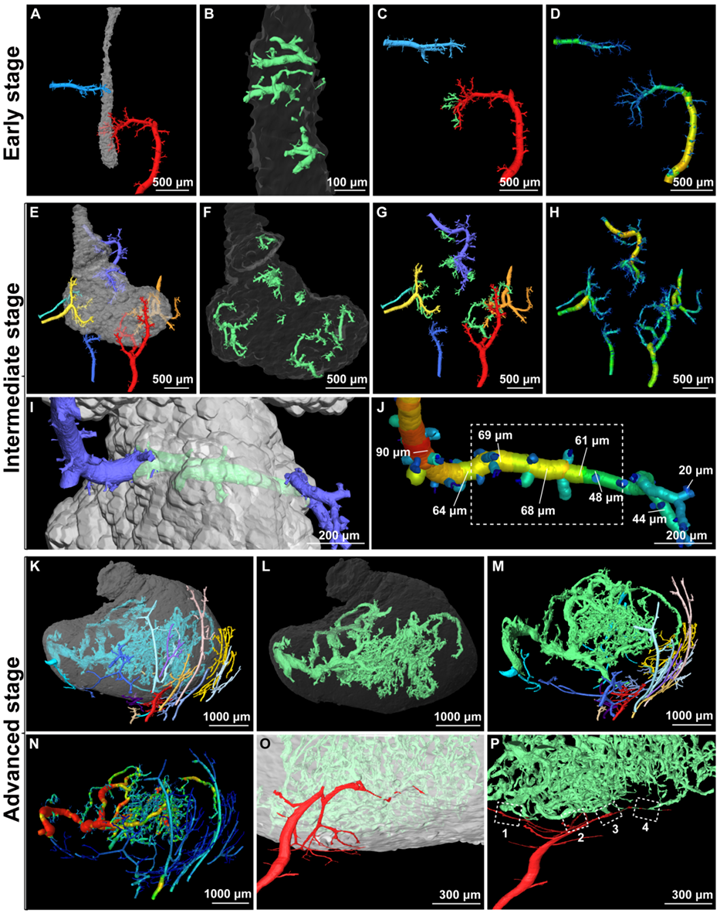
图 1 胶质瘤脑血管病理重塑规律
该研究发现,肿瘤侵袭性、血管网络结构和血管新生方式均呈现显著的时空异质性。早期肿瘤边界呈现模糊、粗糙的特征,而晚期则演变为清晰、光滑的边界形态;在血管网络方面,肿瘤血管系统经历显著的病理重塑过程,表现为结构紊乱程度逐渐加剧,分支模式趋于无序,管腔直径异常增大以及微血管网络退化等特征(图1)。此外,全肿瘤尺度的纳米粒子3D分布可视化结果显示,纳米粒子不仅能通过肿瘤毛细血管渗透入脑实质,还可借助肿瘤重塑后的大直径血管跨越血脑屏障(图2)。
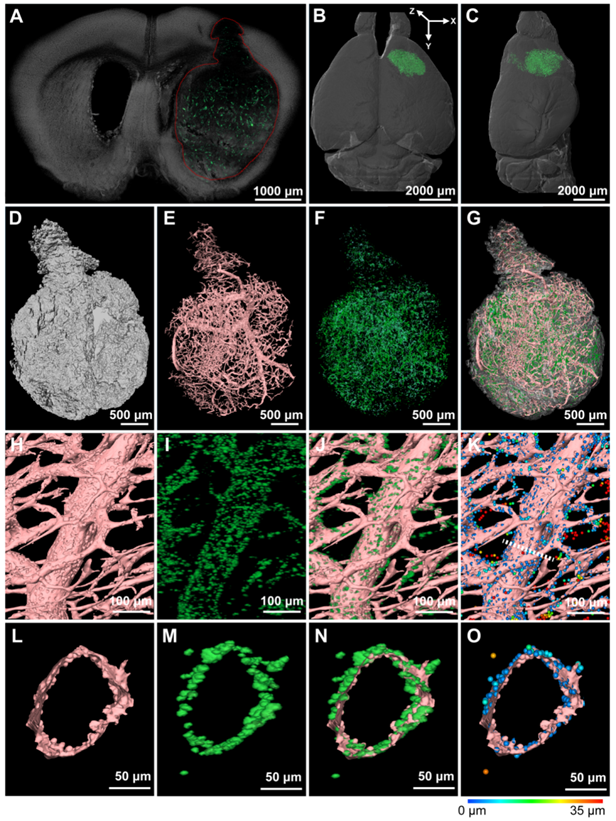
图 2 纳米粒子在脑胶质瘤组织的3D分布规律
原文链接:https://www.science.org/doi/10.1126/sciadv.adw8330
2. 高精度全景肝脏图谱:三维解码肝纤维化的病理特征

在2025年3月24日发表于Advanced Science上的研究中,临港实验室殷宪振团队与中国科学院上海药物张小川团队合作,成功构建全球首套高精度完整肝脏3D病理图谱(图3),首次实现从宏观器官到微观细胞的跨尺度全景呈现,系统破译肝纤维化等疾病的“空间密码”,标志着肝脏病理研究正式迈入3D时代。
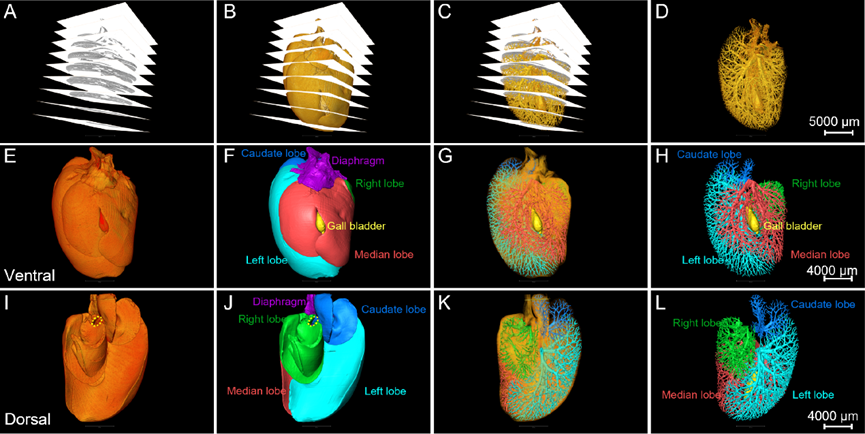
图3.高精度完整肝脏3D重建
该研究首次实现对整个肝脏器官(包括各叶、胆囊)及其内部关键结构(中央静脉、门静脉、动脉、胆管、肝血窦、肝细胞)的完整3D重建(图4),成功捕获了传统二维切片难以观测的精细结构,如胆管周围微血管丛,这为跨尺度解析肝脏解剖结构和病理变化提供了可靠平台。研究团队以肝纤维化为研究对象,采用四氯化碳(CCl₄)诱导的小鼠模型,结合高精度 3D 病理图谱开展分析,借助 3D 空间定位,发现肝脏损伤呈非均质性分布,即中央静脉周围区域的肝细胞脂肪变性和胶原沉积更为显著,而门静脉区域的病变相对轻微。基于 3D 图谱的定量分析实现了病理特征空间关联的精确定量,进而揭示出一个关键规律:肝细胞脂肪变性的严重程度与距中央静脉的空间距离密切相关,表现为距离越近病变越严重,且这种关联不受中央静脉直径大小的影响。这种病理特征在 3D 空间中的特异性分布,不仅为深入解析肝纤维化的发病机制提供了全新关键线索,也为潜在治疗靶点的发现提供了精准的空间坐标。
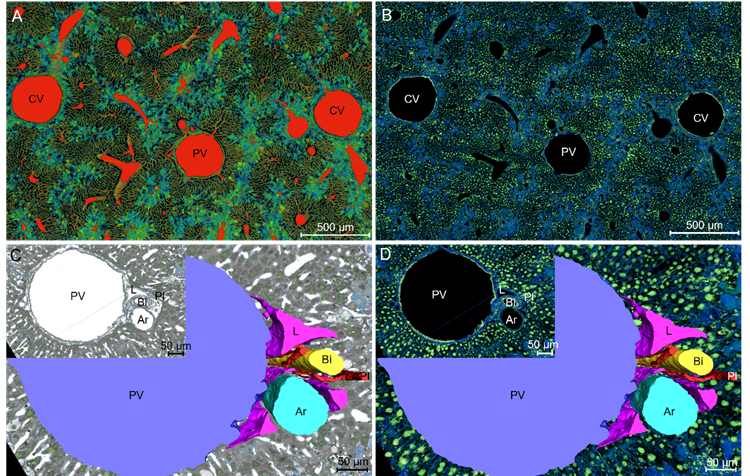
图4.肝脏多结构高精度渲染及脉管提取
该3D病理研究体系具有良好的通用性,目前已成功应用于肝纤维化研究,未来有望推广至其他肝脏疾病(如肝炎、肝癌、脂肪肝)及复杂器官系统疾病的基础研究与临床诊断。该体系将提升疾病诊断的准确性,为疾病机制研究、靶点发现、疗效评估及个体化治疗提供3D空间信息支持,推动诊疗策略的优化。
原文链接:https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202502744
3. 开展气管靶向递药系统设计与跨尺度3D表征

临港实验室殷宪振团队与中国科学院上海药物研究所张继稳团队合作,提出了“结构药剂学”的新理念,揭示了结构与质量之间的关系,并将该理念拓展至生命组织层面。结合跨尺度三维(3D)成像,递药系统在体内的分布规律被精准刻画,这不仅为纳米递药系统的设计与优化提供了坚实基础,也为个体化诊疗提供了新的思路与技术支撑。相关研究在2025年6月5日发表于《美国化学会-纳米》,并被选为封面文章。
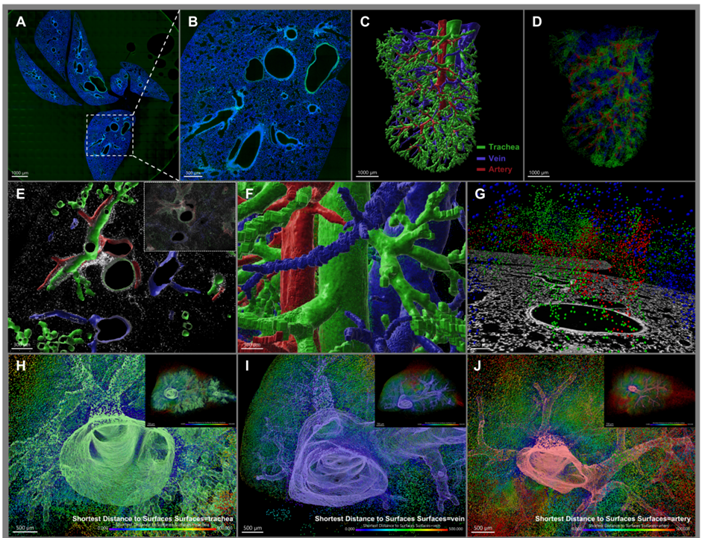
图 5 GCC-Rh110经尾静脉注射后的肺部3D空间分布
肺部病理微环境具有高度的时空异质性,相关药物递送面临多重挑战。传统二维(2D)研究手段难以跨尺度表征纳米制剂在肺部的生物分布,极大限制了递药系统的靶向性评价。为突破该瓶颈,研究团队开展了面向生命体的“结构药剂学”研究,利用交联环糊精纳米网格材料(GCC),结合单颗粒示踪与3D病理图谱,进行了从制剂结构到生理结构的跨尺度关联分析,在单细胞分辨率上实现了对纳米粒在气管外周的精准定位,并观察到其3D空间分布表现出显著的气管外壁聚集特征(图5)。此外,研究团队在脂多糖诱导的支气管炎模型中开展3D药效学评价,结合机器学习识别并提取气管周围的炎性细胞体积分布,实现多级气管的虚拟内窥及气管壁厚的精准定量,完成从制剂结构到生理结构的跨尺度关联分析,为肺部疾病的精准治疗及药效评估提供新策略(图6)。
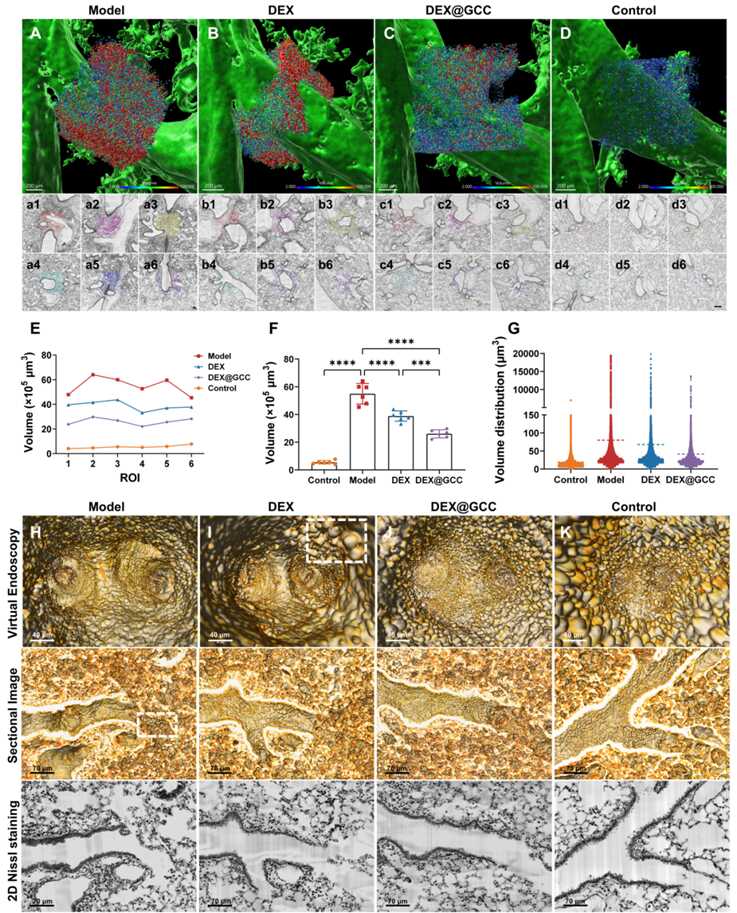
图 6 气管周围炎症细胞和肺泡上皮细胞的3D可视化
原文链接:https://pubs.acs.org/doi/10.1021/acsnano.5c06694
3D病理研究已跨越传统认知边界——它不仅重构了我们对疾病空间本质的理解,更重塑了药物递送的核心范式。综上,临港实验室影像学团队整合多模态、跨尺度成像技术,构建了覆盖脑、肝脏、肺脏等多器官的 3D 病理评价体系。该体系拥有“3D可视化 - 跨尺度关联 - AI 量化”三大核心能力,不仅为递药系统设计提供了“结构 - 功能 - 疗效”的3D研究范式,还有望推动病理学从“静态描述”向“动态时空建模”的跨越式发展。
附件下载:



