STTT | 临港实验室合作使用长读长测序技术构建胆囊癌转录组图谱,发现新转录本与肿瘤细胞的妥珠单抗抗药性有关
2025年2月14日,临港实验室魏武研究团队与上海交通大学医学院附属仁济医院刘颖斌团队联合在Signal Transduction and Targeted Therapy期刊上在线发表了题为“Full-Length Transcriptome Atlas of Gallbladder Cancer Reveals Trastuzumab Resistance Conferred by ERBB2 Alternative Splicing”的研究论文。

胆囊癌是一种恶性程度高的消化道肿瘤,预后极差。肿瘤细胞的转录组常常出现失调,RNA可发生异常剪接,产生多种新的异构体和蛋白变异体,促进肿瘤进展。本研究利用先进的长读长全长转录组测序技术,对胆囊正常组织、肿瘤组织和细胞系进行了全面分析,构建了首个胆囊全长转录组图谱。研究者鉴定到了一种命名为ERBB2 i14e的新转录本,其编码一种新的功能蛋白。该蛋白在胆囊癌中高表达。ERBB2 i14e在剪接因子ESRP1/2的调控下产生,其编码的i14e肽段可显著促进增殖。进一步研究发现该新变体会在曲妥珠单抗的治疗中被显著上调,并介导了药物耐受。进一步在患者来源的异种移植瘤模型实验中验证发现,抗义寡核苷酸阻断ERBB2 i14e可增强肿瘤对曲妥珠单抗及其药物缀合物的敏感性。总的来说,本研究展示了长读长测序在肿瘤基础研究中的价值,发现了肿瘤细胞针对以曲妥珠单抗为基础的治疗策略的耐药机制,为该治疗方案的改善提供了新的策略。
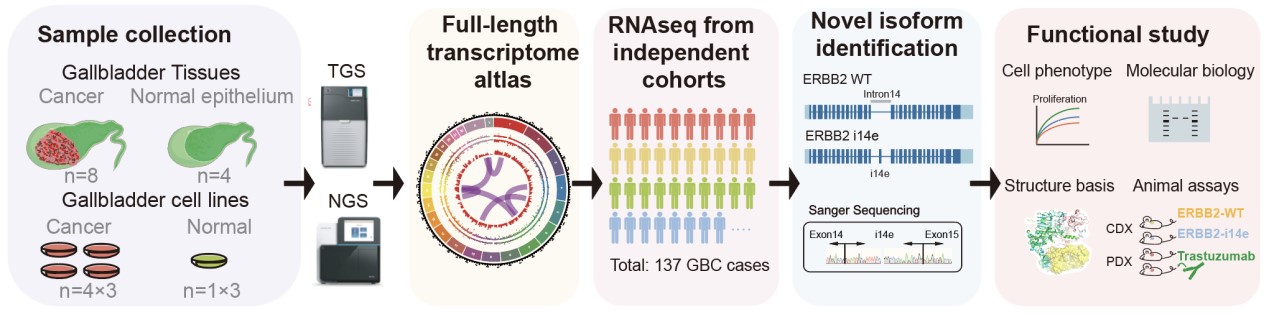
研究设计示意图
研究团队针对胆囊癌这一恶性程度极高预后极差的疾病开展研究。通过对胆囊组织、胆囊癌组织、胆囊癌细胞系、非癌症的胆囊癌细胞系进行高深度的转录组Pacbio CCS高通量测序,并整合构建出胆囊系统的转录组图谱。为胆囊-胆囊癌系统的基础研究提供了重要的参考,使用构建的图谱与大批量胆囊癌转录组测序数据,发现受体酪氨酸激酶是变化最为显著的基因家族之一,其中来自ERBB2基因的转录本是最为突出的、高表达且最具多态性的。
通过批量的ERBB2的新转录本筛选,聚焦到了一种新的ERBB2转录本,该转录本的特点在于14号内含子上出现了新的外显子,因此该转录本被命名为ERBB2 i14e(intron 14 derived exon),该新蛋白具有很强的促进细胞增殖的能力,并且其在肿瘤中显著升高。深入的机制研究发现,新的外显子产生的蛋白肽段位于ERBB2胞外的IV号结构域,其能增强ERBB2与ERBB3的相互作用以及下游的信号转导。同时更值得注意的是,该肽段也破坏了曲妥珠单抗与ERBB2的结合界面,导致表达ERBB2 i14e蛋白的肿瘤细胞无法被曲妥珠单抗所影响。
进一步的研究发现,该新转录本的出现并非是基因组突变所影响的,是肿瘤细胞的转录后调节失常所引起的。而调节ERBB2 i14e出现的关键剪接因子是ESRP1/2,干扰ESRP1/2上的UGG-rich基序会显著影响ERBB2 i14e的产生,同时ESRP1/2也是胆囊癌中显著失调的剪接因子之一。通过在患者来源的类器官和PDX模型上的实践,发现ERBB2 i14e是针对ERBB2的靶向治疗耐药的机制之一,并且通过翻译寡核苷酸干预ERBB2 i14e的产生可以显著提升德曲妥珠单抗对胆囊癌的治疗效果。
简单来说,该研究通过一个典型案例,充分凸显出长读长测序在肿瘤研究中的作用。以全长转录组测序为基础的研究工作在癌症发展和耐药性研究中的转化医学和临床治疗价值。同时研究发现了ERBB2的一个新的转录异构体,从机制上揭示了紊乱的肿瘤转录组干预癌细胞增殖和耐药性的方式,为胆囊癌的诊断生物标志物和治疗靶点提供了新的方向。
上海交通大学医学院附属仁济医院胆胰外科刘颖斌教授、临港实验室魏武研究员、上海交通大学医学院附属仁济医院胆胰外科李茂岚教授、上海市肿瘤研究所黎彦璟研究员为本文通讯作者。上海交通大学医学院附属仁济医院胆胰外科王子逸住院医师、中国科学院营养与健康所高莉博士、上海交通大学医学院附属仁济医院胆胰外科贾子衡博士、刘立果住院医师与顾澳博士为本文的共同第一作者。本研究得到国家自然科学基金等项目的资助。
附件下载:



