Science Advances | 临港实验室合作利用全肺图谱在单细胞水平上对纳米粒和肿瘤进行跨尺度追踪
肿瘤的异质性和复杂的微环境是导致药物递送系统的靶向性和疗效不佳的重要原因。探究肿瘤病灶在各阶段的血管、细胞构筑以及细胞外基质通透性的变化规律,深化对肿瘤异质性和肿瘤治疗的结构认识,有助于解决药物递送的底层难题。然而,受限于器官、肿瘤组织和纳米粒子之间明显的尺度差异,为表征肿瘤环境和药物递送系统之间相互作用,克服成像尺度与分辨率之间的矛盾开发高精度的可视化方法,是一项艰巨的任务。本研究基于显微光学断层扫描/荧光显微光学断层扫描系统(MOST/fMOST),在三维空间、单细胞水平上,构建B16F10小鼠肺转移瘤病理图谱,阐明纳米载体在肿瘤和临近组织的时空分布规律,对其在肿瘤组织的渗透行为及靶向效率进行定量评价。本研究构建了一种全新的纳米载体靶向效率的高精度可视化评估方法,突破现有肿瘤成像方法及瘤内纳米载体可视化技术的瓶颈和局限性,为纳米递药系统的设计和开发提供新的策略。
2023年8月2日,临港实验室殷宪振团队联合中国科学院上海药物研究所张继稳团队,在Science Advances上发表了题为“Cross-scale tracing of nanoparticles and tumors at the single-cell level using the whole-lung atlas”的研究论文。

MOST系统在全器官尺度具有较高的分辨率,边切片、边成像,无需特异性标记,通过灰度和形态学差异即可实现多种病理结构的同步可视化。为分析肺部肿瘤微环境的结构变化,评价生理结构的受损程度,研究人员基于MOST系统完成全肺肿瘤病理结构的跨尺度同步可视化,在三维空间、单细胞水平上全面精准地表征肺转移瘤的病理特征。包括对肺气管高精度内窥、解析病灶对周围肺泡挤压和侵袭的规律、全肺图谱内的肿瘤病灶分类,以及各阶段肿瘤血管结构参数的定量分析等。肿瘤血管系统在发展过程中经历着显著的三维结构变化,血管网络的纵向分支点不断增加,横向分支点不断减少,逐渐趋于成熟、复杂、混乱。肿瘤自身新生血管在生长、成熟过程中,汲取宿主血管营养,不断增粗、变长,愈发错综复杂、紊乱。考虑肿瘤微环境和异质性的综合影响对认知肿瘤非常重要,结构参数的定量有助于更准确地理解复杂的肿瘤微环境(图1)。
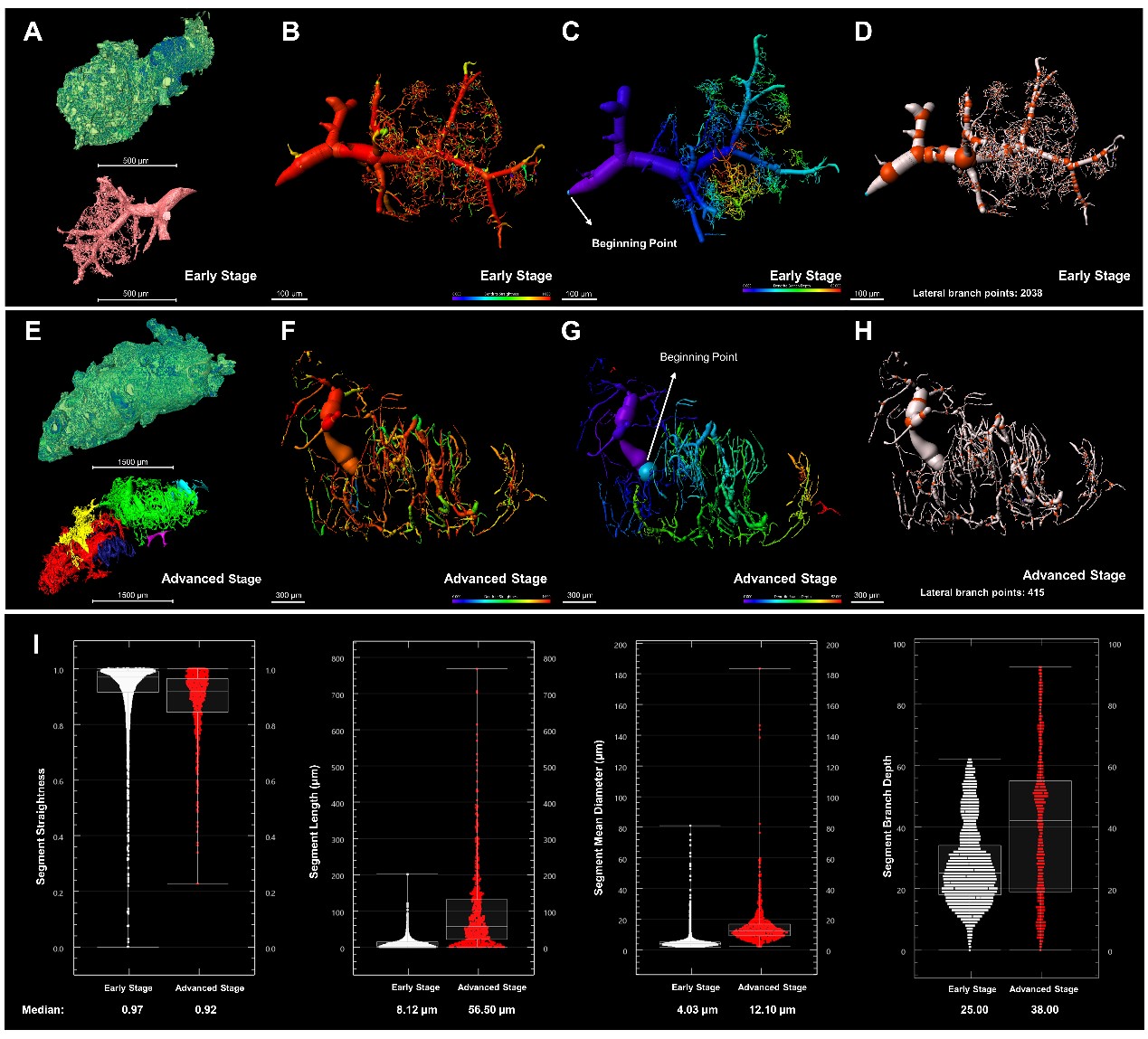
图 1 C57BL/6小鼠全肺图谱血管系统的高精度三维可视化和定量:(A)早期肺转移瘤及其血管系统。三维拟合后,早期转移灶血管片段的平直度(B)和分支深度(C)。(D)早期血管片段的分支点。(E)晚期肺转移瘤及其血管系统。三维拟合后,晚期转移灶血管片段的平直度(F)和分支深度(G)。(H)晚期血管片段的分支点。(I)肺转移灶(早期-白色,晚期-红色)血管片段结构参数定量分析:平直度、长度、平均直径、分支深度。
随后,研究人员以环糊精金属有机骨架为基本单元,设计、制备并表征了可主动靶向肿瘤组织的荧光纳米载体Nano-COF-A488-cRGD,该载体可被多种肺泡组织典型细胞摄取。fMOST系统适用于荧光样本,结合实时碘化丙啶(PI)复染,进行双通道荧光成像,为实现给药后荧光微粒在病灶、器官的空间分布提供可能。基于此,本研究定量考察了Nano-COF-A488-cRGD在肿瘤病灶中的渗透、聚集行为,发现粒子在全肺瘤内分布与肿瘤内部纤维化程度有关:粒子在纤维化较轻微的病灶中更密集,而在严重纤维化的病灶中的分布尚不及正常肺泡。纳米制剂的肿瘤内渗行为需要依靠肿瘤自身的血管网络,血管结构的形态变化同样会影响粒子的瘤内分布:随着肿瘤的发展,血管系统的结构会不断被破坏,导致颗粒在肿瘤组织中的积聚更加明显(图2)。
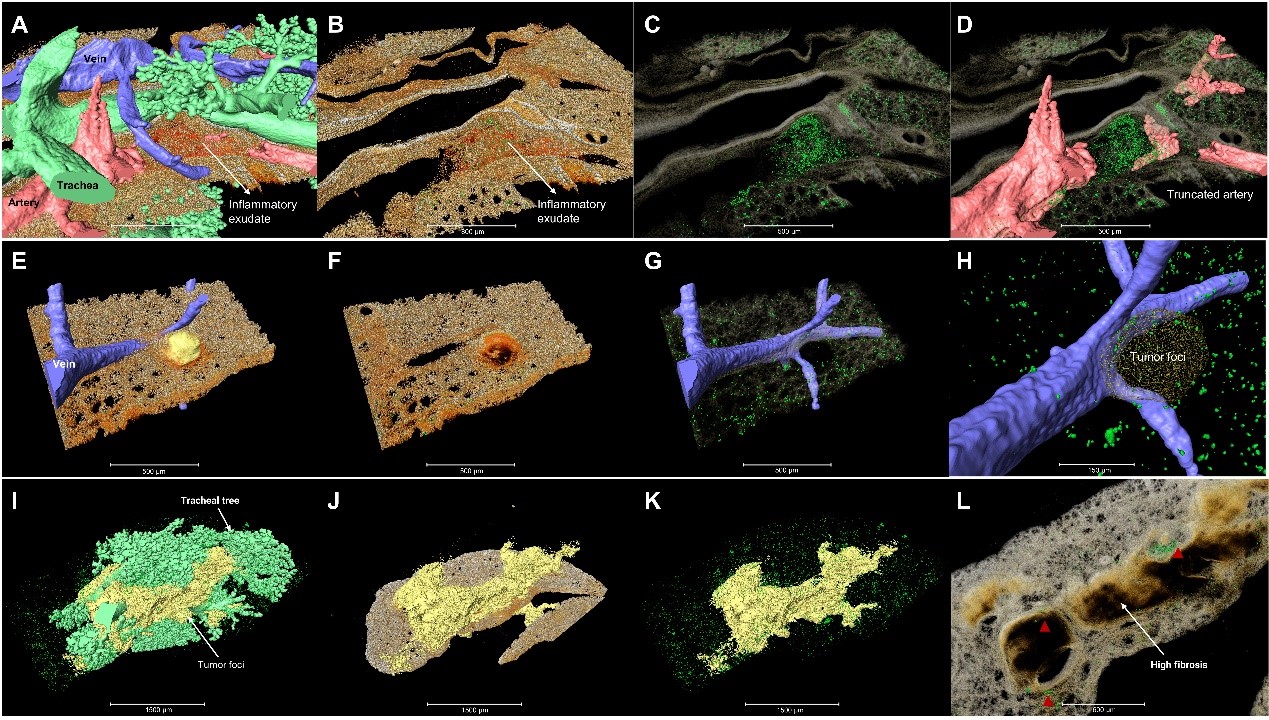
图 2 纳米载体Nano-COF-A488-cRGD在不同部位肿瘤病灶的三维空间分布:(A)侵袭动脉的肿瘤组织,及气管、动静脉的三维重构。纳米粒在炎症渗出液(B-C)和被截断的宿主动脉(D)中的三维空间分布;(E)侵袭静脉的肿瘤组织,以及静脉和肿瘤病灶的三维重构。(F)肿瘤病灶严重的纤维化。纳米粒的三维空间分布(G)及其放大图(H);(I)侵袭气管的肿瘤组织,气管树和肿瘤病灶的三维重构,肿瘤病灶的三维结构(J),肿瘤病灶内的纳米粒分布(K)。(L)纳米粒在纤维化程度不同的区域分布,用红色三角形标识。
纳米制剂的分布和肿瘤的结构密切相关,对肿瘤的早期治疗有着重要意义,确认肿瘤血管网的结构有助于优化给药策略。同时,由可视化结果评价纳米制剂的靶向效率,通过肿瘤脉管结构异常化程度来评价药效,具有较强的可行性和创新性。本研究揭示了肺转移瘤的三维结构变化,弥补了肿瘤跨尺度成像分析方法学上的缺失。构建了一种全新的荧光纳米载体可视化方法,为揭示靶向递送系统的药物分布和药效学评价奠定坚实的基础。MOST系统也可采集到淋巴和神经的结构信息,特异性抗体染色结合转基因动物,以及荧光标记的肿瘤细胞建模,可通过fMOST系统研究淋巴系统,揭示肿瘤微环境与免疫系统及神经系统的相互作用。同时,此方法还可应用到其他的药物递送载体、疾病模型和给药方式中,在跨尺度三维空间、单细胞水平构建肿瘤病理图谱,具有重大意义和广泛需求。
中国科学院上海药物研究所博士研究生曹泽颖和临港实验室研究助理赵艳丽为本研究的共同第一作者;本研究由临港实验室殷宪振研究员和中国科学院上海药物研究所张继稳研究员共同指导。中国科学院上海药物研究所MOST及图像融合分析平台参与了MOST/fMOST数据的收集。本研究获得了战略性国际科技创新合作重点专项、临港实验室开放课题和江西省创新领军人才短期计划的资助。本研究中的细胞摄取及定量评价得到了国家蛋白质科学中心(上海高等研究院)的大力支持。
附件下载:



